Batterier. Regneeksempler
 Batterier er elektrokemiske strømkilder, der efter afladning kan oplades ved hjælp af elektrisk strøm fra en oplader. Når ladestrømmen løber i batteriet, opstår der elektrolyse, hvorved der dannes kemiske forbindelser på anoden og katoden, der var på elektroderne i batteriets indledende driftstilstand.
Batterier er elektrokemiske strømkilder, der efter afladning kan oplades ved hjælp af elektrisk strøm fra en oplader. Når ladestrømmen løber i batteriet, opstår der elektrolyse, hvorved der dannes kemiske forbindelser på anoden og katoden, der var på elektroderne i batteriets indledende driftstilstand.
Elektrisk energi, når den oplades i et batteri, omdannes til en kemisk form for energi. Når den aflades, bliver den kemiske form for energi elektrisk. Det kræver mere energi at oplade et batteri, end man kan opnå ved at aflade det.
Spændingen i hver celle i et bly-syre-batteri efter opladning af 2,7 V bør ikke falde til under 1,83 V ved afladning.
Den gennemsnitlige spænding af et nikkel-jern batteri er 1,1 V.
Batteriets lade- og afladningsstrøm er begrænset og indstillet af producenten (ca. 1 A pr. 1 dm2 af pladen).
Mængden af elektricitet, der kan trækkes fra et opladet batteri, kaldes batteriets ampere-timekapacitet.
Batterier er også kendetegnet ved energi- og strømeffektivitet.Energiafkastet er lig med forholdet mellem den energi, der modtages under afladningen, og den energi, der bruges på at oplade batteriet: ηen = Araz / Azar.
For et bly-syre batteri ηen = 70% og for et jern-nikkel batteri ηen = 50%.
Strømudgangen er lig med forholdet mellem mængden af elektricitet modtaget under afladning og mængden af elektricitet, der forbruges under opladning: ηt = Q gange / Qchar.
Bly-syre-batterier har ηt = 90% og jern-nikkel-batterier ηt = 70%.
Batteriberegning
1. Hvorfor er batteriets strømafkast større end energiafkastet?
ηen = Araz / Azar = (Op ∙ Ip ∙ tp) / (Uz ∙ Iz ∙ tz) = Op / Uz ∙ ηt.
Energiafkastet er lig med strømafkastet ηt ganget med forholdet mellem afladningsspændingen og ladespændingen. Da forholdet Uр / U3 <1, så ηen <ηt.
2. Et blybatteri med en spænding på 4 V og en kapacitet på 14 Ah er vist i fig. 1. Tilslutningen af pladerne er vist i fig. 2. Parallelkobling af pladerne øger batterikapaciteten. To sæt plader er forbundet i serie for at øge spændingen.
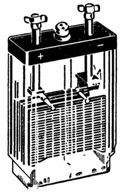
Ris. 1. Bly-syre batteri
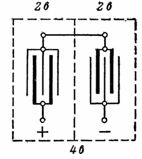
Ris. 2. Tilslutning af pladerne på et bly-syrebatteri til en spænding på 4 V
Batteriet oplades på 10 timer med en strøm på Ic = 1,5 A og aflades på 20 timer med en strøm på Ip = 0,7 A. Hvad er strømeffektiviteten?
Qp = Ip ∙ tp = 0,7 ∙ 20 = 14 A • h; Qz = Iz ∙ tz = 1,5 ∙ 10 = 15 A • h; ηt = Qp / Qz = 14/15 = 0,933 = 93%.
3. Batteriet oplades med en strøm på 0,7 A i 5 timer. Hvor længe vil den aflade med en strøm på 0,3 A med en strømudgang ηt = 0,9 (fig. 3)?
Ris. 3. Figur og diagram for eksempel 3
Mængden af elektricitet, der bruges til at oplade batteriet, er: Qz = Iz ∙ tz = 0,7 ∙ 5 = 3,5 A • h.
Mængden af elektricitet Qp, der frigives under afladning, beregnes med formlen ηt = Qp / Qz, hvorfra Qp = ηt ∙ Qz = 0,9 ∙ 3,5 = 3,15 A • h.
Afladningstid tp = Qp / Ip = 3,15 / 0,3 = 10,5 timer.
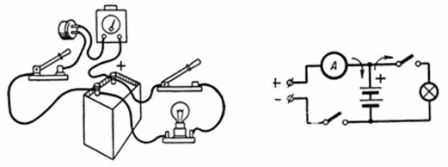
4. 20 Ah-batteriet blev fuldt opladet inden for 10 timer fra lysnettet via en selensretter (fig. 4). Ensretterens pluspol er forbundet med batteriets pluspol under opladning. Med hvilken strøm oplades batteriet, hvis strømeffektiviteten ηt = 90%? Med hvilken strøm kan batteriet aflades inden for 20 timer?
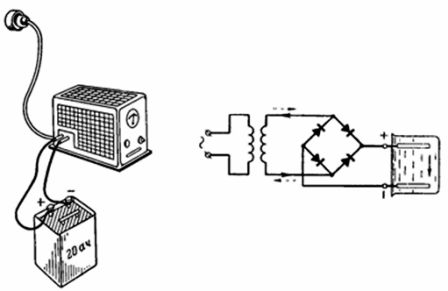
Ris. 4. Figur og diagram for eksempel 4
Batteriets ladestrøm er: Ic = Q / (ηt ∙ tc) = 20 / (10 ∙ 0,9) = 2,22 A. Tilladt afladningsstrøm Iр = Q / tr = 20/20 = 1 A.
5. Et akkumulatorbatteri bestående af 50 celler oplades med en strøm på 5 A. en battericelle 2,1 V, og dens indre modstand rvn = 0,005 Ohm. Hvad er batterispændingen? Hvad er etc. c. skal have en ladningsgenerator med intern modstand rg = 0,1 Ohm (fig. 5)?
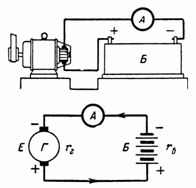
Ris. 5. Figur og diagram for eksempel 5
D. d. C. batteri er lig med: Eb = 50 ∙ 2,1 = 105 V.
Batteriets indre modstand rb = 50 ∙ 0,005 = 0,25 Ohm. D. d. S. generator er lig med summen af e. etc. med batterier og spændingsfald i batteri og generator: E = U + I ∙ rb + I ∙ rg = 105 + 5 ∙ 0,25 + 5 ∙ 0,1 = 106,65 V.
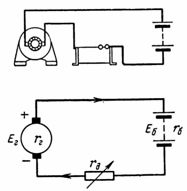
6. Batteriet består af 40 celler med intern modstand rvn = 0,005 Ohm og f.eks. etc. s. 2,1 V. Batteriet oplades med strøm I = 5 A fra generatoren, f.eks. etc. medsom er 120 V og den indre modstand rg = 0,12 Ohm. Bestem den ekstra modstand rd, generatorens effekt, ladningens nyttige effekt, effekttabet i den ekstra modstand rd og strømtabet i batteriet (fig. 6).
Ris. 6. Beregning af akkumulatoren
Find yderligere modstand vha Kirchhoffs anden lov:
F.eks. = Eb + rd ∙ I + rg ∙ I + 40 ∙ rv ∙ I; rd = (Eg-Eb-I ∙ (rg + 40 ∙ rv)) / I = (120-84-5 ∙ (0,12 + 0,2)) / 5 = 34,4 / 5 = 6,88 Ohm …
Da e. osv. c. Når batteriet er opladet, er cellens EMF ved begyndelsen af opladningen 1,83V, derefter ved begyndelsen af opladningen, med en konstant ekstra modstand, vil strømmen være mere end 5 A. For at opretholde en konstant opladning strøm, er det nødvendigt at ændre den ekstra modstand.
Effekttab i den ekstra modstand ∆Pd = rd ∙ I ^ 2 = 6,88 ∙ 5 ^ 2 = 6,88 ∙ 25 = 172 W.
Effekttab i generatoren ∆Pg = rg ∙ I ^ 2 = 0,12 ∙ 25 = 3 W.
Strømtab i batteriets indre modstand ∆Pb = 40 ∙ rvn ∙ I ^ 2 = 40 ∙ 0,005 ∙ 25 = 5 W.
Generatorens tilførte effekt til det eksterne kredsløb er Pg = Eb ∙ I + Pd + Pb = 84 ∙ 5 + 172 + 5 = 579 W.
Nyttig ladeeffekt Ps = Eb ∙ I = 420 W.